في 24 أغسطس 2021، أعلنت شركة كارا ثيرابيوتكس وشريكتها التجارية فيفور فارما عن موافقة إدارة الغذاء والدواء الأمريكية على دواء ديفيليكفالين (كورسوفا™)، وهو أول دواء من نوعه من فئة مُحفزات مستقبلات كابا الأفيونية، لعلاج مرضى الفشل الكلوي المزمن (الحكة المتوسطة/الشديدة مع علاج غسيل الكلى)، ومن المتوقع إطلاقه في الربع الأول من عام 2022. وقّعت كارا وفيفور اتفاقية ترخيص حصرية لتسويق كورسوفا™ في الولايات المتحدة، واتفقتا على بيعه لشركة فريزينيوس ميديكال. وتبلغ حصة كارا وفيفور من إيرادات المبيعات 60% و40% على التوالي، باستثناء فريزينيوس ميديكال؛ حيث تبلغ حصة فريزينيوس ميديكال من إيرادات المبيعات 50% لكل منهما.
الحكة المصاحبة لمرض الكلى المزمن (CKD-aP) هي حكة معممة تحدث بتواتر وكثافة عاليين لدى مرضى الكلى المزمن الذين يخضعون لغسيل الكلى. تحدث الحكة لدى حوالي 60%-70% من المرضى الذين يخضعون لغسيل الكلى، ويعاني 30%-40% منهم من حكة متوسطة إلى شديدة، مما يؤثر بشكل خطير على جودة الحياة (مثل ضعف جودة النوم) ويرتبط بالاكتئاب. لا يوجد علاج فعال للحكة المصاحبة لمرض الكلى المزمن حتى الآن، وتساعد موافقة دواء دايفيليكفالين على سد الفجوة الكبيرة في الاحتياجات الطبية. تستند هذه الموافقة إلى تجربتين سريريتين محوريتين من المرحلة الثالثة في طلب تسجيل دواء جديد: بيانات إيجابية من تجربتي KALM-1 وKALM-2 في الولايات المتحدة وحول العالم، وبيانات داعمة من 32 دراسة سريرية إضافية، والتي تُظهر أن دواء KORSUVA™ جيد التحمل.
قبل فترة وجيزة، صدرت أخبار سارة من الدراسة السريرية لدواء دايفيليكفالين في اليابان: في 10 يناير 2022، أعلنت شركة كارا أن شريكتيها مارويشي فارما وكيسي فارما أكدا استخدام حقن دايفيليكفالين في اليابان لعلاج الحكة لدى مرضى غسيل الكلى. في المرحلة الثالثة من التجارب السريرية، تم تحقيق الهدف النهائي الأولي. تلقى 178 مريضًا دواءً لمدة 6 أسابيع من دايفيليكفالين أو دواءً وهميًا، وشاركوا في دراسة تمديد مفتوحة لمدة 52 أسبوعًا. تحسنت نقطتا النهاية الأوليتان (التغير في درجة الحكة على مقياس التصنيف العددي) والثانويتان (التغير في درجة الحكة على مقياس شيراتوري لشدة المرض) بشكل ملحوظ عن خط الأساس في مجموعة دايفيليكفالين مقارنةً بمجموعة الدواء الوهمي، وكانا جيدي التحمل.
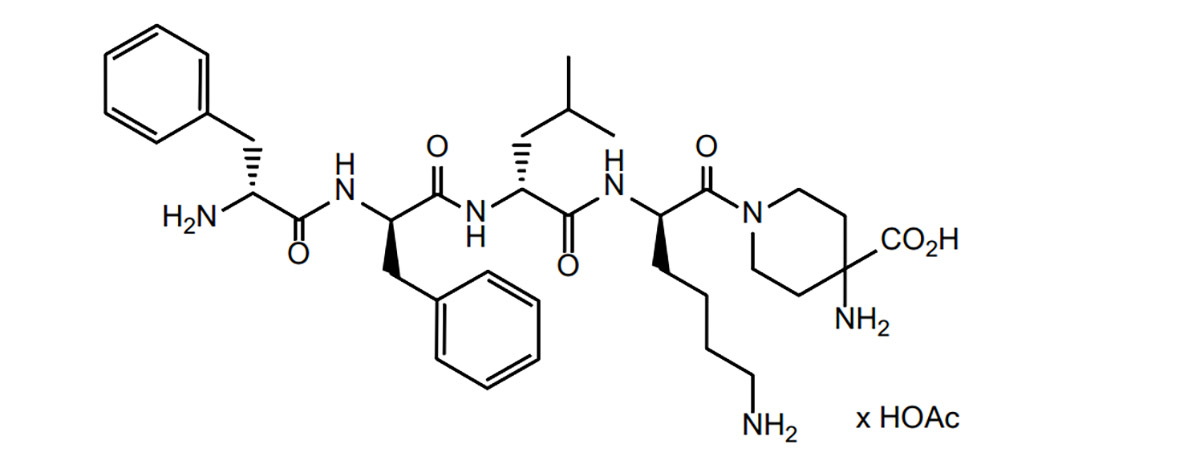
ديفيليكفالين هو فئة من ببتيدات الأفيون. بناءً على ذلك، درس معهد أبحاث الببتيدات الأدبيات المتعلقة بببتيدات الأفيون، ولخص الصعوبات والاستراتيجيات المتعلقة بها في تطوير الأدوية، بالإضافة إلى الوضع الحالي لتطوير الأدوية.
وقت النشر: ١٧ فبراير ٢٠٢٢